Afbeelding in de hoofding: Redox cartoon. Bron: https://www.youtube.com/watch?v=_HZCMuw2BG4 (Jwalpa Coaching Classes)
Om van dode materie levende wezens te maken, heb je metabolisme nodig. In 0.3. hebben we gezien dat CHNOPS de elementen zijn die in de opbouw en werking van levende cellen domineren (koolstof, waterstof, stikstof, zuurstof, fosfor, zwavel). Al die elementen moeten door levende wezens opgenomen worden uit de omgeving , en ingebouwd worden in het (cel)lichaam in de vorm van biomoleculen. Het meest centrale element is echter koolstof. Om de basis van metabolisme te begrijpen, gaan we ons concentreren op dit centrale element.
Oxidatie en reductie van koolstof
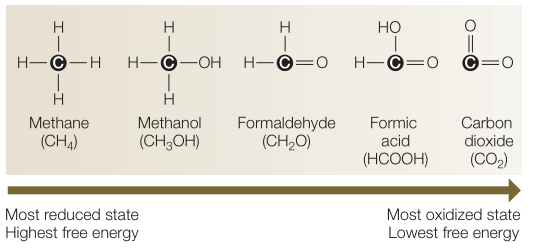
De koolstof die in ons Zonnestelsel (in elders in het heelal) meest voorkomt is de geoxideerde vorm CO2 of CO. Wanneer het leven deze koolstof wil gebruiken om het cellichaam op te bouwen, dan moet die koolstof gereduceerd worden. Wat bedoelen we met ‘gereduceerde’ en geoxideerde’ koolstof?
Koolstof is een atoom met vier elektronen in de buitenste ‘schil’. Elk atoom wil er liever 8 hebben in de buitenste schil, want dat is de meest stabiele toestand. Daarom gaat koolstof graag chemische verbindingen vormen om vier elektronen van andere atomen te kunnen delen. In CO2 bijvoorbeeld, gaat koolstof aan beide zijden zelf twee elektronen aan de binding met zuurstof geven, en zuurstof zelf deelt er ook twee. op die manier kom je aan een totaal van 8 elektronen, zowel voor de zuurstof- als voor de koolstofatomen.

Omdat in de binding tussen zuurstof en koolstof de beide partner-atomen niet dezelfde zijn, is er altijd eentje die de gedeelde elektronen meer naar zich toe trekt. Zuurstof is meer ‘elektronegatief’ dan koolstof. Dat betekent dat zuurstof de gedeelde elektronen meer naar zich toe trekt. Dus in deze C-O verbinding kan je zeggen dat koolstof elektronen ‘verliest’ aan zuurstof. Een koolstof atoom dat elektronen is kwijt geraakt noemen we ‘geoxideerd’. De elektronegativiteit van koolstof is 2,55 en die van zuurstof is 3,44.
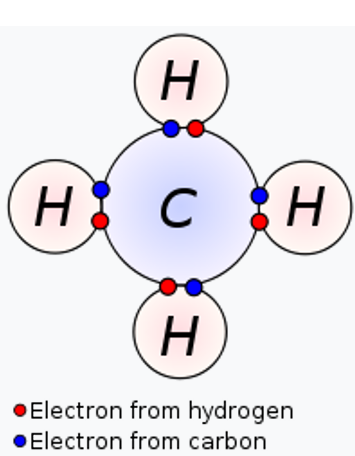
Vergelijk dat nu eens met een koolstof atoom dat in de CH4 molecule zit.
Waterstof heeft een elektronegativiteit van 2,20. Dat is dus minder dan koolstof (2,55). In deze C-H verbinding zal koolstof deze keer de gedeelde elektronen naar zich toe trekken. In dit geval heeft koolstof dus elektronen ‘gewonnen’ (in plaats van kwijt geraakt), en is die dus gereduceerd. De koolstof heeft in deze molecule dus meer negatieve lading naar zich toe getrokken (meer negatief is een reductie).
Als je geoxideerde koolstof wil reduceren, dan moet je normaalgezien energie toevoegen. Terwijl het oxideren van reeds eerder gereduceerde koolstof energie opbrengt. Dat is precies waar het leven gebruik van maakt. Het leven gaat in de regel (toch zeker op Aarde) energie uit de omgeving gebruiken om geoxideerde koolstof te gaan reduceren. Daarna gaat dat leven die gereduceerde koolstof terug oxideren en de energie die daaruit komt opslaan om te gebruiken voor allerlei eigen levensprocessen. Het bekendste aardse voorbeeld hiervan is fotosynthese. Het leven gebruikt zonne-energie om de koolstof van CO2 uit de lucht te reduceren, en daar bijvoorbeeld glucose van te maken (C6H12O6). Daarna wordt een deel van die glucose terug geconsumeerd: de koolstof wordt terug geoxideerd dus. Bij de oxidatie van die glucose-koolstoffen komt energie vrij, dat een levende cel gaat oogsten en opslaan in de ATP molecule. Die energie-molecule wordt later gebruikt voor zowat alles wat een levende cel wil doen.
Redox reacties als basis voor leven
De nobelprijswinnaar Albert Szent-Györgyi (een biochemicus) zei ooit: “Life is nothing else than an electron looking for a place to rest”. Hij bedoelde daarmee dat leven gebaseerd is op die verandering van geoxideerde koolstof naar gereduceerde koolstof, en weer terug. Het elektron heeft dan ‘rust gevonden’ als het terug van de koolstof afgeraakt is en bijvoorbeeld weer naar zuurstof gegaan is. ‘Redox’ is de afkorting van Reductie-Oxidatie. Elke vorm van leven heeft dit als meest essentiële activiteit in haar metabolisme, en haalt er de nodige ‘levensenergie’ uit.
Om het reductie-gedeelte van de redox reacties uit te voeren moet een organisme ergens een elektron vinden om aan de koolstof af te geven. De molecule die gebruikt wordt hiervoor kan vanalles zijn, en wordt de electron donor genoemd. Bij de oxidatie van koolstof zal het organisme het elektron willen afgeven aan een elektron acceptor. Ook daarvoor kunnen verschillende moleculen gebruikt worden. We zullen later meerdere voorbeelden hiervan tegenkomen.