Image dans l’en-tête : dessin animé Redox. Source : https://www.youtube.com/watch?v=_HZCMuw2BG4 (Jwalpa Coaching Classes)
Pour transformer la matière morte en êtres vivants, tu as besoin d’un métabolisme. En 0.3., nous avons vu que les CHNOPS sont les éléments qui dominent dans la construction et le fonctionnement des cellules vivantes (carbone, hydrogène, azote, oxygène, phosphore, soufre). Tous ces éléments doivent être prélevés par les êtres vivants dans l’environnement , et intégrés dans le corps (de la cellule) sous forme de biomolécules. Cependant, l’élément le plus central est le carbone. Pour comprendre les bases du métabolisme, nous allons nous concentrer sur cet élément central.
Oxydation et réduction du carbone
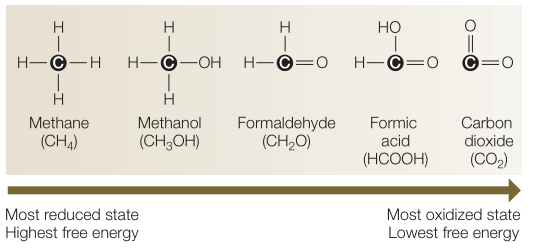
Le carbone que l’on trouve le plus souvent dans notre système solaire (et ailleurs dans l’univers) est la forme oxydéeCO2 ou CO. Si la vie veut utiliser ce carbone pour construire le corps cellulaire, ce carbone doit être réduit. Qu’entend-on par carbone « réduit » et « oxydé » ?
Le carbone est un atome dont la « coquille » extérieure contient quatre électrons. Tous les atomes préfèrent en avoir huit dans la coquille extérieure, car c’est l’état le plus stable. C’est pourquoi le carbone aime former des liaisons chimiques pour partager les quatre électrons d’autres atomes. Dans leCO2, par exemple, le carbone va donner deux électrons à la liaison avec l’oxygène des deux côtés, et l’oxygène lui-même en partage deux.

Parce que dans la liaison entre l’oxygène et le carbone, les deux atomes partenaires ne sont pas les mêmes, il y en a toujours un qui attire davantage à lui ces électrons partagés. L’oxygène est plus « électronégatif » que le carbone. Cela signifie que l’oxygène attire davantage les électrons de la molécule (ceux qui sont partagés) vers lui. Dans ce composé C-O, on peut donc dire que le carbone perd des électrons au profit de l’oxygène. Un atome de carbone qui a perdu des électrons est dit « oxydé ». L’électronégativité du carbone est de 2,55 et celle de l’oxygène de 3,44.
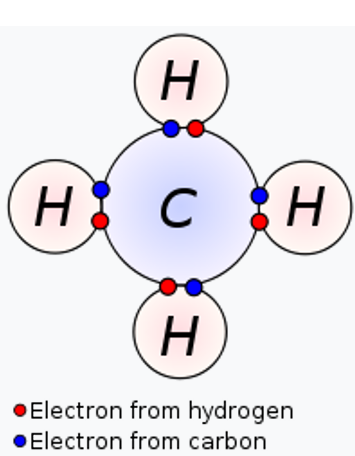
Compare maintenant cela à un atome de carbone contenu dans la molécule de CH4.
L’hydrogène a une électronégativité de 2,20. Elle est donc inférieure à celle du carbone (2,55). Dans ce composé C-H, le carbone attirera cette fois les électrons partagés vers lui. Dans ce cas, le carbone a donc gagné (plutôt que perdu) des électrons, et est donc « réduit ». Dans cette molécule, le carbone a donc attiré à lui une charge plus négative (une charge plus négative est une réduction).
En règle générale, si tu veux réduire le carbone oxydé, tu dois ajouter de l’énergie. Alors que l’oxydation du carbone déjà réduit ajoute de l’énergie. C’est exactement ce dont la vie tire parti. En règle générale (du moins sur Terre), la vie va utiliser l’énergie de l’environnement pour commencer à réduire le carbone oxydé. Ensuite, cette vie va oxyder à nouveau ce carbone réduit et stocker l’énergie qui en résulte pour l’utiliser dans toutes sortes de processus vitaux. L’exemple terrestre le plus connu est la photosynthèse. La vie utilise l’énergie solaire pour réduire le carbone duCO2 de l’air et le transformer, par exemple, en glucose (C6H12O6). Une partie de ce glucose est ensuite consommée à nouveau : le carbone est donc oxydé à nouveau. L’oxydation de ces carbones de glucose libère de l’énergie, qu’une cellule vivante va récolter et stocker dans la molécule d’ATP. Cette molécule d’énergie est ensuite utilisée pour à peu près tout ce que la cellule vivante veut faire.
Les réactions d’oxydoréduction à la base de la vie
Le prix Nobel Albert Szent-Györgyi (biochimiste) a dit un jour : « La vie n’est rien d’autre qu’un électron qui cherche un endroit où se reposer ». Il voulait dire par là que la vie est basée sur le passage du carbone oxydé au carbone réduit, et vice-versa. L’électron a ensuite « trouvé le repos » lorsqu’il a quitté le carbone et est retourné à l’oxygène, par exemple. Redox » est l’abréviation de réduction-oxydation. C’est l’activité la plus essentielle du métabolisme de toute forme de vie, qui en tire l' »énergie vitale » nécessaire.
Pour effectuer la partie réduction des réactions d’oxydoréduction, un organisme doit trouver un électron quelque part pour le donner au carbone. La molécule utilisée pour cela peut être n’importe quoi, et on l’appelle le donneur d’électrons. Lors de l’oxydation du carbone, l’organisme doit donner l’électron à un accepteur d’électrons. Différentes molécules peuvent également être utilisées à cette fin. Nous en verrons plusieurs exemples plus loin.